 Stimulation cérébrale profonde dans le traitement de la maladie de Parkinson
Stimulation cérébrale profonde dans le traitement de la maladie de Parkinson
V. Stéréotaxie, choix techniques et implications pratiques
La stimulation cérébrale profonde utilise la méthodologie stéréotaxique pour la mise en place des électrodes de stimulation.
Si les principes sont toujours identiques, il existe une large palette de moyens techniques et technologiques pour mettre en œuvre cette chirurgie.
Le but de ce chapitre est de donner au lecteur quelques notions de base sur les choix techniques qui lui sont offerts, leurs implication concernant la méthode ainsi que quelques clefs pour s’assurer d’une précision suffisante pour insérer les électrodes dans des structures de petite taille et profondes.
Les choix étant multiples et en partie fonction du plateau technique disponible au sein de son établissement, chaque équipe chirurgicale se doit de se doter d’un système d’assurance qualité permettant de s’assurer de la précision suffisante des moyens employés.
L’utilisation de fantômes, une validation de chacun des outils (dont l’imagerie) mais également un process de vérification de « sa propre » précision applicative (c’est-à-dire la précision finale prenant en compte toutes les composantes de la chirurgie) apparaît indispensable à la méthodologie stéréotaxique.
Exemple des 2 fantômes utilisés au CHU d’Amiens (A gauche le fantôme dédié à l’imagerie d’Elekta®, à droite, le fantôme créé pour évaluer la précision applicative de l’acte. Le fantôme permet la réalisation de tous les mode de recalage avec tous les imageries pré et per opératoires actuellement disponibles)
Enfin, les auteurs de ce chapitre ne pourront que vivement recommander l’utilisation d’une imagerie per opératoire de qualité, seule garante d’un positionnement des électrodes adaptées. Les techniques imageries intra opératoires sont variables d’un centre à un autre mais seul cette information permet réellement au chirurgien de progresser et ainsi d’améliorer (grâce à un retour d’informations suite à chaque chirurgie) sa technique opératoire au cours du temps.
Il conviendra ensuite de s’assurer de la conformité de ces résultats cliniques aux résultats de la littérature apparaît une démarche essentielle afin de proposer une chirurgie adaptée aux besoins de nos populations.
*a. L’imagerie
Toutes les modalités d’imagerie produisent une information morphologique, parfois fonctionnelle voire même métabolique mais également une information géométrique.
Chaque type d’imagerie a des avantages et des inconvénients. Les choix du chirurgien sont fonction de ses buts et de son plateau technique.
Il faudra retenir deux éléments de base pour l’imagerie stéréotaxique(23) :
1) la nécessité d’une absence de mouvement pendant l’acquisition (tout mouvement faisant perdre l’information géométrique)
2) la nécessité d’imager à la fois la cible mais également le référentiel stéréotaxique (fiduciaires du cadre de la boîte de repérage, fiduciaires osseux, ...)
En neurochirurgie stéréotaxique, l’image est utilisée comme outil chirurgical, le chirurgien se devant d’évaluer la qualité de son outil et de vérifier que l’information apportée par cette dernière lui permet d’accomplir son acte opératoire de manière sûre et reproductible.
Nous présenterons les différentes imageries disponibles pour la planification et le contrôle per opératoire.
![]() L’amplificateur de Brillance(32). Il s’agit d’une imagerie 2D. Ses avantages sont sa simplicité d’utilisation, son faible coût. Il s’agit malheureusement d’une imagerie présentant une déformation dite en "coussinet" nécessitant un traitement de l’image spécifique si on désire l’utiliser pour guider les instruments. Il existe également un facteur d’agrandissement lié à la proximité de la source rendant la représentation dans l’espace des structures difficiles. Enfin, cette imagerie ne permet de voir que le crâne et les objets radio-opaques. Il s’agit donc d’une imagerie pouvant être utilisée uniquement pour le contrôle de la position des électrodes à l’aide de mires adaptées pour le cadre utilisé. Ce type de contrôle restera grossier dans le sens où elle ne permettra pas de mesurer l’erreur de position de l’électrode.
L’amplificateur de Brillance(32). Il s’agit d’une imagerie 2D. Ses avantages sont sa simplicité d’utilisation, son faible coût. Il s’agit malheureusement d’une imagerie présentant une déformation dite en "coussinet" nécessitant un traitement de l’image spécifique si on désire l’utiliser pour guider les instruments. Il existe également un facteur d’agrandissement lié à la proximité de la source rendant la représentation dans l’espace des structures difficiles. Enfin, cette imagerie ne permet de voir que le crâne et les objets radio-opaques. Il s’agit donc d’une imagerie pouvant être utilisée uniquement pour le contrôle de la position des électrodes à l’aide de mires adaptées pour le cadre utilisé. Ce type de contrôle restera grossier dans le sens où elle ne permettra pas de mesurer l’erreur de position de l’électrode.
Les auteurs conseillent vivement d’utiliser un autre moyen de contrôle permettant de mesurer l’erreur géométrique, ainsi de mesurer / évaluer à chaque procédure sa précision et si possible prévoir une amélioration continue de sa procédure.
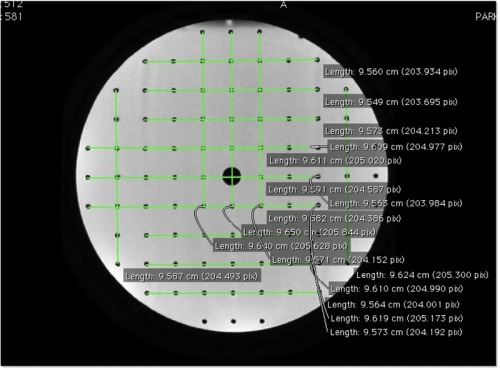
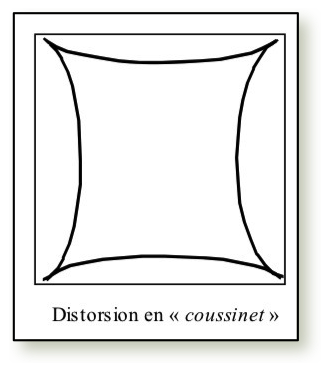
Illustration de la déformation en coussinet et des mires de vérifications disponibles avec le système Elekta®
![]() La téléradiographie(5) consiste en la réalisation de clichés radiographiques dans deux plans strictement orthogonaux (face et profil). La source est placée à 5 m, ce qui permet de limiter le facteur d’agrandissement. L’acquisition de ces clichés se fait après ventriculographie permettant de mouler les ventricules et si besoin après artériographie et veinographie permettant de voir les vaisseaux.
La téléradiographie(5) consiste en la réalisation de clichés radiographiques dans deux plans strictement orthogonaux (face et profil). La source est placée à 5 m, ce qui permet de limiter le facteur d’agrandissement. L’acquisition de ces clichés se fait après ventriculographie permettant de mouler les ventricules et si besoin après artériographie et veinographie permettant de voir les vaisseaux.
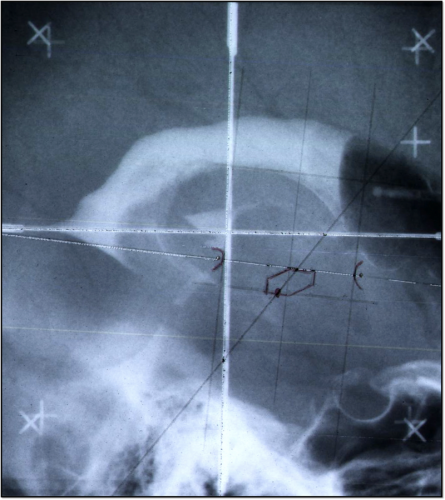
Illustration de l’erreur géométrique avec une ventriculographie
L’avantage de ces clichés est l’absence de distorsion des images (le capteur de réception des images est plan). L’acquisition se fait dans un espace strictement orthogonal, cartésien. Le calcul de la situation de la cible en x,y,z par rapport à un repère fixe (obligatoirement un cadre de stéréotaxie) est fiable. Enfin, le facteur d’agrandissement résiduel peut même être pris en charge par certains navigateurs actuels, ce qui fait de cette imagerie la plus précise d’un point de vue géométrique avec le scanner.
Cette modalité d’imagerie est encore utilisée dans quelques centres en neurochirurgie fonctionnelle pour des cibles de neuromodulation - cible au sein d’une anatomie normale non modifiée par un syndrome de masse- car cette technique permet de parfaitement visualiser les repères Ca-Cp (commissure blanche antérieure et postérieure), la ligne médiane, les parois du troisième ventricule52. De plus, la méthode de détermination de la cible "Talairach - Guiot" permet une détermination statistique de la cible proportionnelle aux dimensions des repères intracrâniens visibles grâce à la ventriculographie (longueur de la ligne bi-commissurale ca-cp ; hauteur du thalamus, largeur du 3è ventricule). L’utilisation du diagramme de Guyot permet une détermination plus fiable de la cible stéréotaxique que les données brutes des atlas stéréotaxiques. Enfin, la présence de la téléradiographie en per opératoire permet lors de procédures de SCP de réaliser un véritable processus de contrôle qualité per opératoire, permettant de vérifier (et si besoin corriger) en per opératoire que ce qui a été planifié est bien ce qui est réalisé5,51.
Diagramme de guyot et détermination de la cible stéréotaxique sur les clichés télé-radiographiques.
Contrôles télé-radiographique per opératoire. Les repères intracrâniens permettent la définition de la cible selon ses coordonnées statistiques. Le contrôle per opératoire permet de s’assurer que les électrodes se situent bien en regard de la cible planifiée.
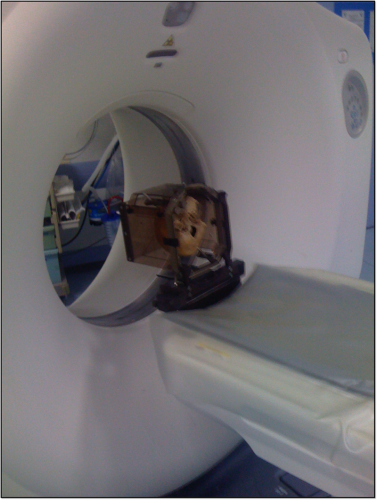
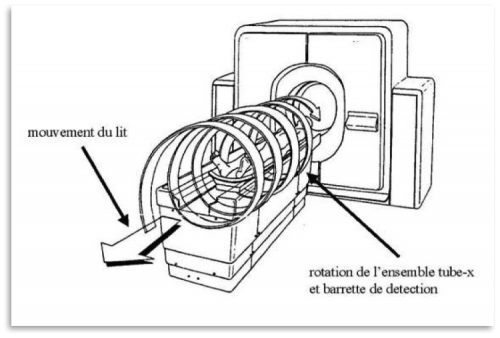
- Le TDM ou scanner(23,21) consiste à calculer une reconstruction 3D des tissus à partir d’une analyse tomographique obtenue en soumettant le patient au balayage d’un faisceau de rayons X. Cette imagerie n’est pas soumise à distorsion. La précision géométrique est directement en lien avec la taille de la matrice (taille de chaque voxel) et avec l’épaisseur des coupes. L’incertitude de localisation sera directement dépendante de la taille du voxel : A titre d’illustration, avec un champ de vue 212 cm, si la matrice est de 256 * 256, (pixel de 0,83 mm de côté) avec une épaisseur coupe de 1,25mm, la taille du voxel sera de 0,86 mm3. En revanche, si la matrice est de 512*512 (pixel de 0,41 mm, de côté) et l’épaisseur de coupe réduite à 0,6 mm, la taille de chaque voxel sera de 0,1 mm3. Les TDM actuels multi barrettes et spiralés permettent actuellement l’acquisition sur 360° de multiples coupes (de 140 à 400), jointives avec une épaisseur de coupes inférieure à 1mm. Ainsi l’acquisition doit être réalisée avec des coupes contiguës de moins de 1 mm d’épaisseur avec des matrices fines (512*512). Enfin, il persistera une dernière incertitude de Z liée au mouvement de la table lors de l’acquisition des images. Avec l’évolution des technologies, cette erreur résiduelle est de plus en plus limitée.
La résolution de contraste, c’est-à-dire la capacité à montrer une structure et à la différencier d’une autre, est sans comparaison avec la téléradiographie mais reste bien inférieure à l’IRM. Cette modalité d’imagerie a révolutionné la stéréotaxie et a permis la généralisation des biopsies stéréotaxiques. Concernant la SCP, le scanner permet la visualisation du parenchyme cérébral mais pas directement des cibles. Seuls les repères Ca-Cp (ligne bi-commissurale) et la ligne médiane sont facilement visualisables. Ainsi le TDM , tout comme la téléradiographie nécessite l’utilisation de données statistiques pour viser les cibles de neuromodulation.
Lors d’une régistration « framebase » (avec cadre), les fiduciaires de la boîte de repérage seront facilement visibles, permettant de déterminer l’espace stéréotaxique avec précision. Les erreurs résiduelles géométriques en imagerie TDM sont en fait liées à l’épaisseur et l’espacement entre les coupes et la taille de la matrice. Le principal défaut de l’imagerie TDM n’est donc pas sa géométrie mais sa résolution de contraste infiniment moins intéressante que celle de l’imagerie IRM.
Illustration des tests de précision du protocole stéréotaxique sous TDM, ainsi que l’illustration du TDM spiralé. L’erreur géométrique résiduelle est liée à l’épaisseur de coupes et à leur caractère (ou non) jointif. Il persiste une incertitude en z.
Conseil d’acquisition pour un TDM stéréotaxique :
Sous cadre, en s’étant assurer d’une acquisition dans un plan parfaitement axial. TDM cérébral, coupe jointive épaisse de 0,6mm avec un incrément de 0,3mm (durée d’acquisition 30s), une matrice de 512*512 pour un champ de vue de 20*20 cm. On s’assurera que les fiduciaires de la boîte de stéréotaxie sont bien dans le champ d’acquisition.
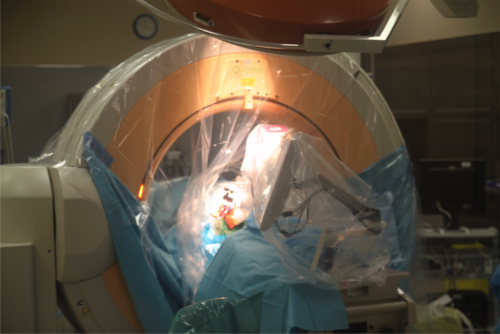
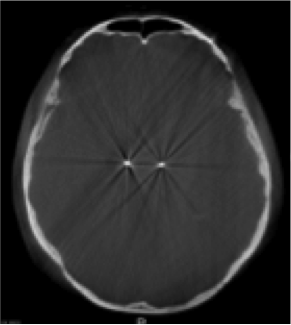
- Scanner à capteur plan (fpCT scan)(22) (dont l’O’arm® Medtronic® est le scanner le plus répandu) sont des amplificateurs de brillance dédiés au bloc opératoire de dernière génération. Il s’agit en réalité de la combinaison d’un mobile de radiographie et d’un anneau (type anneau de scanner). Le système est composé d’un tube à rayon X et d’un détecteur capteur plan monté sur un anneau en vis-à-vis et tournant de manière asservie tout autour du patient. En fonction des scanners disponibles, le scanner se présentera comme un O (L’anneau peut s’ouvrir et se mettre en position arceau en C afin de faciliter son positionnement autour du patient, puis se refermer complètement. Il permet de réaliser une image 2D et une reconstruction en 3D) ou comme un arceau de bloc qui peut réaliser une rotation à 360° autour de l’objet imagé. Pour ces scanners, l’acquisition 3D se faisant en iso-centrique, sur la largeur du capteur plan, il s’agit donc d’une acquisition d’un volume 3D unique qui est redécoupée secondairement par un logiciel. Les scanners à capteurs plans présentent une qualité géométrique supérieure au scanner. En effet, il n’existe pas d’incertitude vis à vis du z. Cette différence fait que la dispersion des erreurs géométrique des scanners à capteur plan est plus faible que celle des scanners multi-barrette, ceci même si la taille du voxel peut être plus grande que celle obtenue avec un scanner multi-barrette28. Cependant, il faut bien comprendre qu’il s’agit de l’évolution d’un amplificateur de brillance et non d’un scanner peropératoire à proprement parler. Les fpCT scan permettent essentiellement d’imager l’os, l’air, les tissus mous, les vaisseaux (en cas de injection de produits de contrastes) et les objets radio-transparents. Il ne permet pas de voir avec précision le parenchyme cérébral.
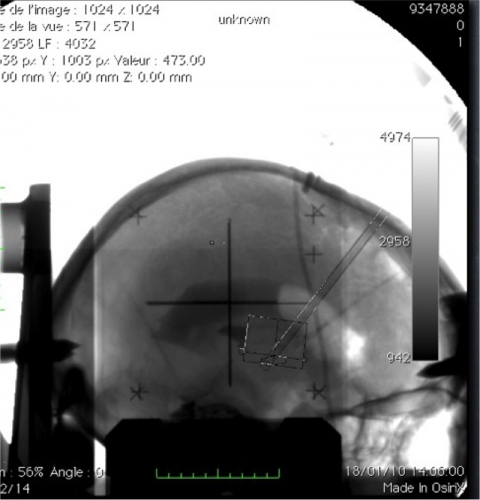
L’O’arm® (Medtronic®) est un scanner à capteur plan. A droite, illustration d’une imagerie obtenue en per opératoire avec un fpCT.
Conseil d’utilisation d’un Scanner à capteur plan en stéréotaxie :
Les scanners à capteur plan se révèlent être des outils de choix pour le contrôle per-opératoire de la position des électrodes. Ils peuvent remplacer avantageusement une téléradiographie.
![]() L’ IRM (Imagerie par résonance magnétique)(23,21,35) est actuellement l’imagerie de choix dans le domaine des neurosciences. L’imagerie IRM présente les avantages d’une excellente résolution de contraste (différenciation substance blanche substance grise, délimitation des tumeurs, visions des sillons, gyri et vaisseaux) et la possibilité d’acquisition d’une imagerie fonctionnelle et métabolique telle l’IRM de perfusion ou spectroscopie. Cependant cette imagerie, basée sur le principe de résonance magnétique nucléaire (c’est-à-dire le couplage entre le moment magnétique du noyau des atomes avec un champ magnétique externe), est soumise « de fait » à une imprécision géométrique ou distorsion.
L’ IRM (Imagerie par résonance magnétique)(23,21,35) est actuellement l’imagerie de choix dans le domaine des neurosciences. L’imagerie IRM présente les avantages d’une excellente résolution de contraste (différenciation substance blanche substance grise, délimitation des tumeurs, visions des sillons, gyri et vaisseaux) et la possibilité d’acquisition d’une imagerie fonctionnelle et métabolique telle l’IRM de perfusion ou spectroscopie. Cependant cette imagerie, basée sur le principe de résonance magnétique nucléaire (c’est-à-dire le couplage entre le moment magnétique du noyau des atomes avec un champ magnétique externe), est soumise « de fait » à une imprécision géométrique ou distorsion.
L’IRM souffre de sérieux problèmes de distorsions, dont les origines sont diverses mais dont les effets se traduisent par des décalages en position (x,y,z) entre les voxels de l’image acquise et ceux de l’objet réel. De nombreuses études ont montré l’importance de ces décalages pouvant atteindre plusieurs millimètres (7 à 8mm !) dans certaines régions du champ de vue imagé. Il en résulte une difficulté à localiser « géométriquement » de manière fiable les structures anatomiques internes. Ces problèmes de distorsion augmentent avec l’intensité du champ magnétique. Ainsi, une IRM 3T présente une meilleure résolution de contraste qu’une IRM 1,5T mais une moins bonne résolution spatiale gênant lors d’un ciblage stéréotaxique. Les raisons de ces distorsions sont fonction de 3 effets : l’effet de susceptibilité magnétique, l’effet de déplacement chimique et la non linéarité des gradients de champ. Les effets de susceptibilité (création d’un champ supplémentaire χ(x).Bo par le milieu magnétique en réponse au champ principal Bo) et de déplacement chimique (fonction de l’environnement chimique des noyaux en résonnance, représente par γ) sont par leur nature des artefacts ne dépendant que de l’objet à imager et non de l’instrument. En particulier, les distorsions sont majeures à chaque interface entre 2 tissus différents et encore plus particulièrement à l’interface air/scalp. De même, les cadres de stéréotaxie sont responsables à des niveaux différents d’une augmentation des distorsions par ces effets. Ces deux effets ne sont pas corrigibles actuellement parce que dépendants de l’objet imagé. Les distorsions liées à la non linéarité du gradient sont responsables de la majeure partie des erreurs de précision géométrique de l’imagerie IRM. La non linéarité du gradient est la résultante du fait que le champ magnétique émis par la bobine (aimant) de l’IRM n’est pas homogène. Ainsi le champ magnétique émis à la périphérie de la bobine est distinct de celui émis au centre. Avant correction, sur une IRM 1,5T, Wang et al. objectivaient des erreurs pouvant aller jusque 9mm, après correction par un algorithme spécifique l’erreur pouvait être diminuée aux alentours de 0,6 mm 55. En effet, ces distorsions en lien avec la non linéarité du gradient sont corrigibles. Une « calibration de l’aimant » et l’adjonction de « patch logiciel » en post acquisition peut sensiblement améliorer la précision géométrique des acquisitions IRM35,55,56,41. Ces erreurs peuvent ainsi être diminuées à moins du demi millimètre (plus précisément jusqu’à à la taille d’un voxel). Il est à noter que l’augmentation de l’intensité du champ magnétique augmente cette erreur. Ainsi, une IRM 3T ne pourra pas être utilisée sans calibration pour des procédures de stéréotaxie.
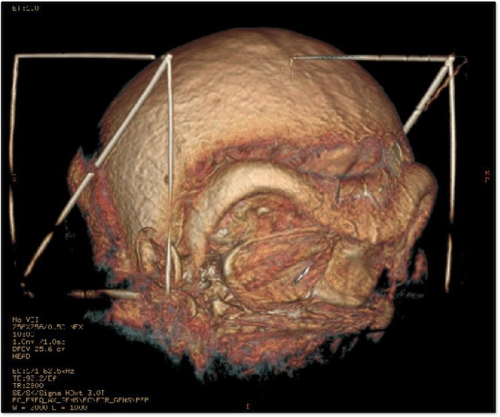
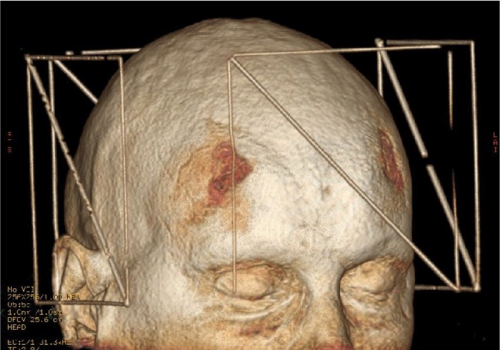
Illustration des erreurs géométriques augmentant à mesure que l’on est à distance du centre de l’aimant. Cette erreur est typiquement liée à la non linéarité du gradient.
Reconstruction 3D de 2 séquences IRM distinctes d’un même patient. A gauche, il s’agit d’une séquence IRM 3T T2 acquise en coronale sans optimisation de l’image, à droite une séquence 3D iso à matrice élevée pour laquelle le travail d’optimisation est commencée. Il faut remarquer que ces 2 séquences après mesures ne présentaient pas les critères de précision géométrique nécessaires pour une utilisation stéréotaxique.
Enfin comme toute imagerie à visée de guidage, une acquisition isotropique et isocentrique en coupe axiale ou acquisition 3D immédiate est indispensable tout comme la nécessité de diminuer au maximum l’épaisseur de coupe et d’obtenir une matrice la plus fine possible (512*512). Enfin l’IRM présente un dernier inconvénient consistant au temps d’acquisition des séries. En effet, un temps plus long est responsable d’une probabilité plus élevée de mouvements de la part du patient en particulier chez les patients atteints d’une pathologie du mouvement. Les erreurs provenant du patient pendant l’acquisition des images peuvent être responsables d’erreurs géométriques majeures.
Il faut cependant comprendre que l’imagerie IRM n’est pas une imagerie homogène en terme de géométrie. Les erreurs géométriques seront présentes et importantes à certains endroits de l’image alors que d’autres portions de l’image pourront se révéler extrêmement fiables géométriquement. Il faut alors que le chirurgien connaisse son imageur, l’optimise avec ses collègues radiologues et physiciens d’IRM afin d’en diminuer les distorsions afin de pouvoir tirer partie des informations données par cette imageur.
Conseils d’utilisation de l’IRM en Stéréotaxie
Les chirurgiens se doivent d’utiliser des imageries dédiées à la SCP, optimisées d’un point de vue géométrique et permettant de voir la cible stéréotaxique. De l’avis des auteurs, l’IRM apporte une information vitale aux gestes stéréotaxiques modernes (l’adaptation de la détermination de la cible selon l’anatomie propre du patient et non sur des données statistiques permettant une visualisation et donc détermination de la cible plus aisée37 et dans les 3 plans de l’espace. Une démarche spécifique d’optimisation des images en particulier IRM apparaît aujourd’hui nécessaire à la démarche stéréotaxique.
Illustration de 2 séquences optimisées pour la SCP. A gauche une séquence en inversion récupération permettant de visualiser, le putamen, le pallidum externe, le pallidum interne et la capsule interne dans les 3 plans de l’espace. A Droite, une séquence 3D Swan HR optimisée pour la visualisation du NST dans les 3 plans de l’espace.
![]() Problèmes liés à la fusion des images : Nombreux chirurgiens utilisent le TDM pour ses qualités géométriques et réalisent la fusion et le recalage avec l’imagerie IRM pour pouvoir déterminer les repères stéréotaxiques et déterminer la cible. Il est important de se rappeler que ce processus mathématique est soumis aux erreurs des algorithmes de fusion/recalage des différents navigateurs (le processus utilisé est le plus souvent le RMS (root mean square - loi des plus faible carré)(31). Cette erreur n’est pas quantifiable en per opératoire. Il persiste toujours une incertitude sur la position exacte de l’électrode dans l’espace stéréotaxique à la fin de l’intervention. Plus l’imagerie tant TDM qu’IRM sera optimisée (faibles distorsions, taille des matrices, faible épaisseur de coupe), plus faible sera l’erreur résultante. Il est important de mettre en place également pour ce processus un système d’assurance qualité afin de s’assurer que l’erreur résultante est minimale.
Problèmes liés à la fusion des images : Nombreux chirurgiens utilisent le TDM pour ses qualités géométriques et réalisent la fusion et le recalage avec l’imagerie IRM pour pouvoir déterminer les repères stéréotaxiques et déterminer la cible. Il est important de se rappeler que ce processus mathématique est soumis aux erreurs des algorithmes de fusion/recalage des différents navigateurs (le processus utilisé est le plus souvent le RMS (root mean square - loi des plus faible carré)(31). Cette erreur n’est pas quantifiable en per opératoire. Il persiste toujours une incertitude sur la position exacte de l’électrode dans l’espace stéréotaxique à la fin de l’intervention. Plus l’imagerie tant TDM qu’IRM sera optimisée (faibles distorsions, taille des matrices, faible épaisseur de coupe), plus faible sera l’erreur résultante. Il est important de mettre en place également pour ce processus un système d’assurance qualité afin de s’assurer que l’erreur résultante est minimale.
 Encyclopædia Neurochirurgica
Encyclopædia Neurochirurgica